Rappelons tout d’abord que tensioactif, détergent, base lavante, agent de surface (en anglais surfactant) désignent, dans le cas présent, le même type de composants. Ce sont des molécules solubles dans l’eau qui possèdent la propriété de s’agréger aux interfaces entre l’eau et d’autres substances peu solubles dans l’eau, en particulier les corps gras. Ces molécules sont dites amphiphiles, c’est-àdire qu’elles sont constituées de deux parties de polarité différente, l’une lipophile (qui peut se lier aux matières grasses) et l’autre hydrophile (qui peut se lier à l’eau). La partie lipophile est apolaire, c’est-à-dire que sa charge électrique (électrostatique) est nulle, alors que la partie hydrophile est polaire (avec une certaine charge électrique).
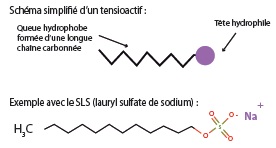
Ils permettent de solubiliser deux phases non miscibles, c’est-à-dire de faire en sorte que deux fluides qui se sépareraient sinon restent mélangés à un niveau « fin », en favorisant leur affinité l’un envers l’autre et donc leur dispersion l’un dans l’autre. En général, l’une des phases est aqueuse (hydrophile et inversement lipophobe) et l’autre grasse (lipophile et inversement hydrophobe). Le meilleur exemple de la non-affinité de ces deux types de phases s’observe lorsqu’on agite un mélange huile et eau : très rapidement les gouttes d’huiles se rassemblent pour « fuir » l’eau et se regroupent en une couche séparée.
Placés en milieu aqueux, les tensioactifs s’orientent de façon à éviter que leur partie hydrophobe soit au contact avec l’eau : soit ils se placent à la surface de l’eau, soit, pour ceux qui sont en solution, ils se rassemblent en amas (micelles) par regroupement de leur partie hydrophobe au centre, la partie hydrophile isolant celle-ci à l’extérieur :*
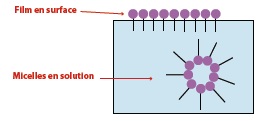
Leur intérêt est varié : action mouillante (étalement d’un liquide sur une surface solide ou augmentation de la vitesse de pénétration dans les corps poreux), moussante (formation de bulles), émulsionnante (formation et stabilisation d’une émulsion), dispersante (stabilité d’une suspension) ou détergente (détachement des saletés de leur support puis dispersion dans l’eau).
L’hydrophilie peut l’emporter sur la lipophilie et vice versa. Pour chaque molécule tensioactive, on peut ainsi définir une HLB (balance hydrophile lipophile) sur une échelle de 1 à 20. Une émulsion huile dans l’eau nécessitera un tensioactif de HLB élevée alors qu’une émulsion eau dans l’huile nécessitera un tensioactif de HLB faible.
Il existe quatre types de composés tensioactifs, classés selon la nature de la partie hydrophile :
● les tensioactifs anioniques : partie hydrophile chargée négativement. HLB relativement élevée car ils ont une tendance hydrophile plus marquée
● les tensioactifs cationiques : partie hydrophile chargée positivement.
● tensioactifs amphotères : ils possèdent à la fois une charge électrique positive et une charge négative, et la charge globale est nulle. HLB élevée.
● tensioactifs non ioniques : la molécule ne comporte aucune charge.

Les tensioactifs anioniques (ex. lauryl sulfate de sodium) sont utilisés comme détergents, savons, agents moussants, humectants, dispersants, mouillants et comme actifs bactériostatiques. Les cationiques (ex. ammoniums quaternaires) ne sont ni bons détergents, ni bons agents moussants mais de bons dispersants des particules solides. Bons bactéricides ou bactériostatiques, ils sont employés dans les désinfectants médicaux, industriels ou domestiques.
Ce sont aussi des agents antistatiques et adoucissants pour le textile et les cheveux. Les amphotères (ex. phospholipides), peu irritants, sont largement employés dans les produits cosmétiques et pharmaceutiques.
Les non-ioniques (ex. esters de glycol ou de glycérol), faiblement toxiques, sont employés en cosmétique et en alimentaire comme détergents, agents mouillants, émulsifiants et parfois moussants. En cosmétique, dont nombre de produits sont des émulsions (nettoyants, crèmes de soin), les tensioactifs sont incontournables dans leur rôle d’émulsifants, sinon ces émulsions décanteraient (les phases aqueuse et grasse se sépareraient).
Et comme dit en introduction, dans leur rôle de détergent (et en même temps d’émulsifiant), ils sont au coeur des produits lavants.


Saleté accrochée sur un support
On notera que la formation de mousse est un effet « secondaire » du pouvoir tensioactif, en emprisonnant de l’air. Si celle-ci favorise une bonne dispersion des corps gras, il est inutile de mousser pour avoir un pouvoir détergent ! Un gel-douche ou un shampooing qui ne mousse pas lave aussi bien !
A l’instar d’autres composants, l’innocuité et l’écologie des bases lavantes s’évalue tout au long de leur cycle de vie : processus de fabrication (origine des matières premières, notamment si les sources sont renouvelables ou non, transformation…), utilisation (risques pour la santé : pouvoir irritant et allergène, toxicité sur le long terme, la toxicité aiguë à court terme étant normalement chose impossible avec la réglementation cosmétique) et devenir après utilisation (biodégradabilité, écotoxicité…).
● Les cationiques sont irritants (surtout pour les yeux) et toxiques pour l’environnement.
● Les anioniques, les plus utilisés car bons détergents et moussant bien, faciles à rincer, sont en général irritants, bien que plus doux que les cationiques.
● Les non-ioniques, avec un faible pouvoir moussant, souvent utilisés comme émulsifiants ou épaississants, sont soupçonnés pour certains d’entre eux (alcools éthoxylés, alcanolamides, alkylphénols éthoxylés) d’être des perturbateurs du système hormonal. Mais certains sont d’origine naturelle et beaucoup plus intéressants.
● Les amphotères, bons détergents et avec un bon pouvoir moussant, ne sont pas ou peu irritants pour les yeux et la peau (ex. bétaïne).
Globalement, les tensioactifs de synthèse, issus de la pétrochimie, peuvent provoquer des irritations et des allergies de la peau. Ce sont des polluants importants, car ils sont peu ou mal biodégradables et libèrent en se décomposant des composés chimiques parfois plus toxiques que le produit initial. Mieux vaut donc choisir des tensioactifs fabriqués à partir de matières premières renouvelables (végétales comme le coprah ou le colza, sucres, acides aminés…) car ceux-ci présentent moins de risques pour la santé et pour l’environnement.
Comme dit à l’instant, toutes les bases lavantes issues de la pétrochimie présentent globalement un risque plus ou moins élevé, pour la santé et/ou l’environnement. Le sodium lauryl sulfate (SLS) est très irritant, au point d’être utilisé comme substance de référence dans les contrôles de tolérance cutanée !
Le sodium laureth sulfate (SLES), moins irritant, est néanmoins obtenu par éthoxylation, un procédé polluant interdit par les cahiers des charges bio et qui peut générer lors de sa fabrication du 1,4-Dioxane, un contaminant classé potentiellement cancérigène. Comme le SLS, il aurait entre autres une toxicité hépatique. Certaines personnes y sont allergiques. Il peut dessécher la peau, altérer sa qualité et la rendre perméable à des substances nocives. Le sodium laureth sulfosuccinate est une molécule plus grande et à ce titre ne pénètre pas la peau, mais issu également de l’éthoxylation, sa fabrication peut donc engendrer aussi du 1,4-Dioxane. L’ammonium lauryl sulfate (ALS), certes autorisé par les cahiers des charges bio (Ecocert/Cosmebio, NaTrue), s’avère néanmoins posséder un pouvoir irritant, qui peut cependant être atténué par certains « co-tensioactifs ». Certaines marques certifiées ont fait le choix de ne pas l’utiliser. Le BDIH ne l’autorise pas.
En bio, les tensioactifs agressifs sont remplacés par des tensioactifs doux, non ioniques. Mais comme sur certains autres sujets, les différentes certifications de cosmétique naturelle et bio ne sont donc pas en accord sur ce thème. Outre l’ALS, c’est également le cas de la cocamidopropyl bétaïne : Ecocert/Cosmebio autorise ce tensioactif doux mais ni le BDIH ni NaTrue, en raison du fait est qu’il est partiellement issu de matières non renouvelables. Son avantage est qu’il adoucit l’ALS.
Le sodium cocoamphoacétate, tensioactif non irritant et non toxique, autorisé par Ecocert/Cosmebio, est par contre aussi interdit à la fois par le BDIH et NaTrue, qui le jugent non compatible avec une vraie orientation naturelle.
Les tensioactifs les plus doux sont les acylglutamates, bases lavantes non ioniques à base d’acides aminés, facilement reconnaissables au terme « glutamate» dans leur nom, comme disodium cocoyl glutamate ou sodium cocoyl glutamate. Mais ils sont plus chers, jusqu’à plus de 10 fois le prix de ceux issus de la pétrochimie ! Ils restent encore assez rares.
Autres tensioactifs très doux, ceux obtenus à partir de sucres et d’huiles végétales, comme le coco glucoside, le lauryl glucoside ou le decyl glucoside, également non ioniques. Ce sont des alkylpolyglycosides (APG), des esters de sucre qui présentent de nombreux avantages comme tensioactifs : matières premières peu coûteuses et renouvelables, aucune toxicité ni pouvoir irritant, aucune odeur, biodégradabilité complète…
Mentionnons aussi le Sodium coco sulfate, également anionique, un dérivé sulfaté (ester) des acides gras de l’huile de coco.
Les infos essentielles du marché bio spécialisé et des EAP, pour tout savoir sur l’actualité des marques, des distributeurs…
Les CGV sont disponibles sur simple demande merci d’utiliser notre formulaire pour nous les demander.
Pour offrir les meilleures expériences, nous utilisons des technologies telles que les cookies pour stocker et/ou accéder aux informations des appareils. Le fait de consentir à ces technologies nous permettra de traiter des données telles que le comportement de navigation ou les ID uniques sur ce site. Le fait de ne pas consentir ou de retirer son consentement peut avoir un effet négatif sur certaines caractéristiques et fonctions.